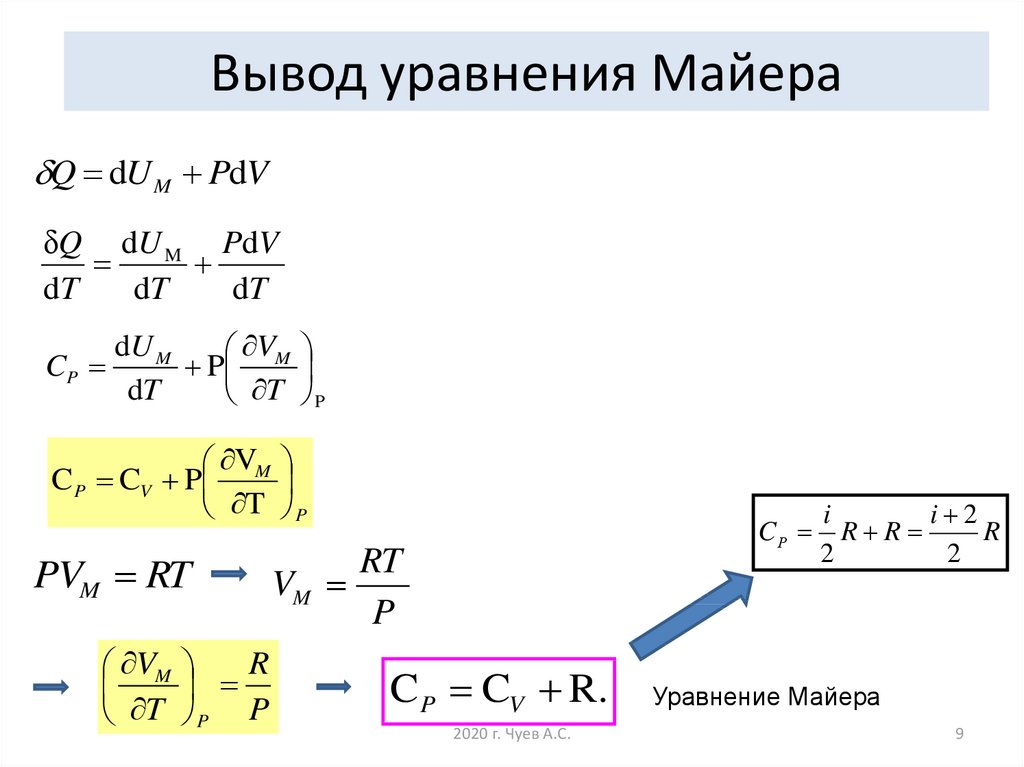
Как вывести уравнение идеального газа
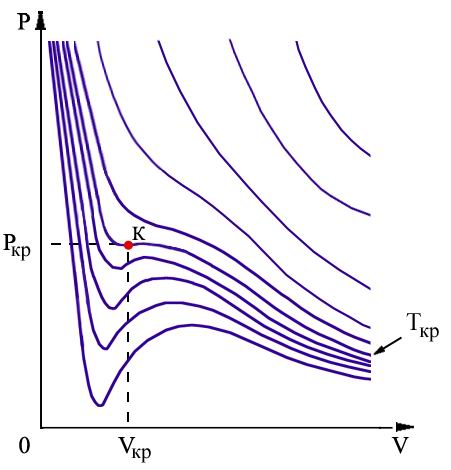
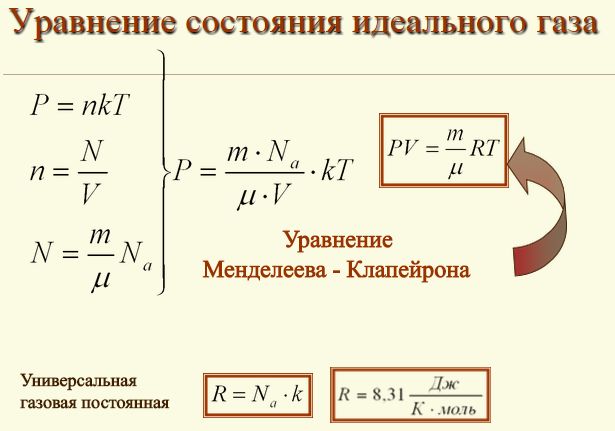
57. Вывод уравнения состояния идеального газа (уравнение Менделеева-Клайперона)
Строго запрещено смотреть анал видео. Крутые - все самые шикарные мамки видео. Мега лучший пердос video. Уравнение, связывающее температуру, давление и объем идеального газа в состоянии теплового равновесия, называют уравнением состояния газа. Соотношение 2 и есть уравнение состояния идеального газа.
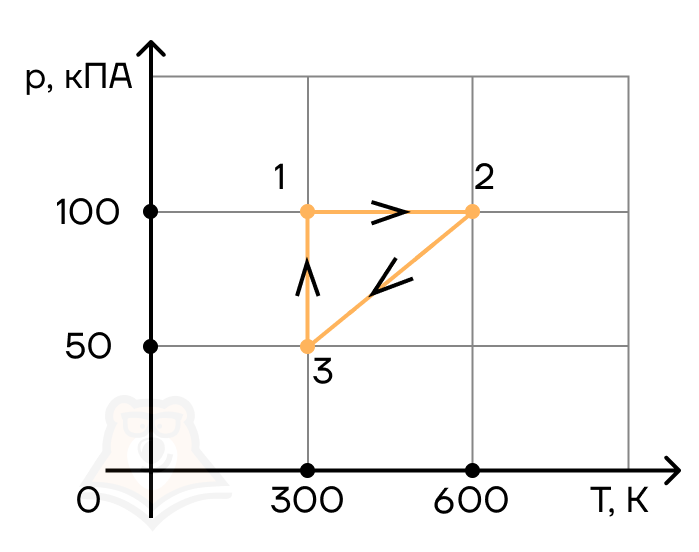

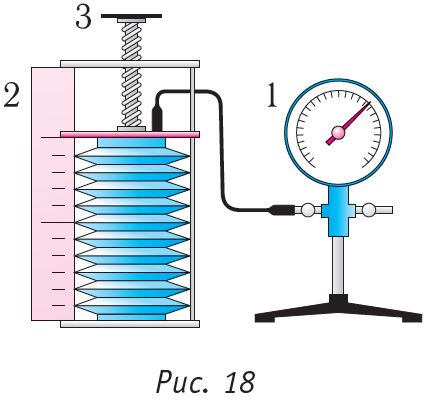
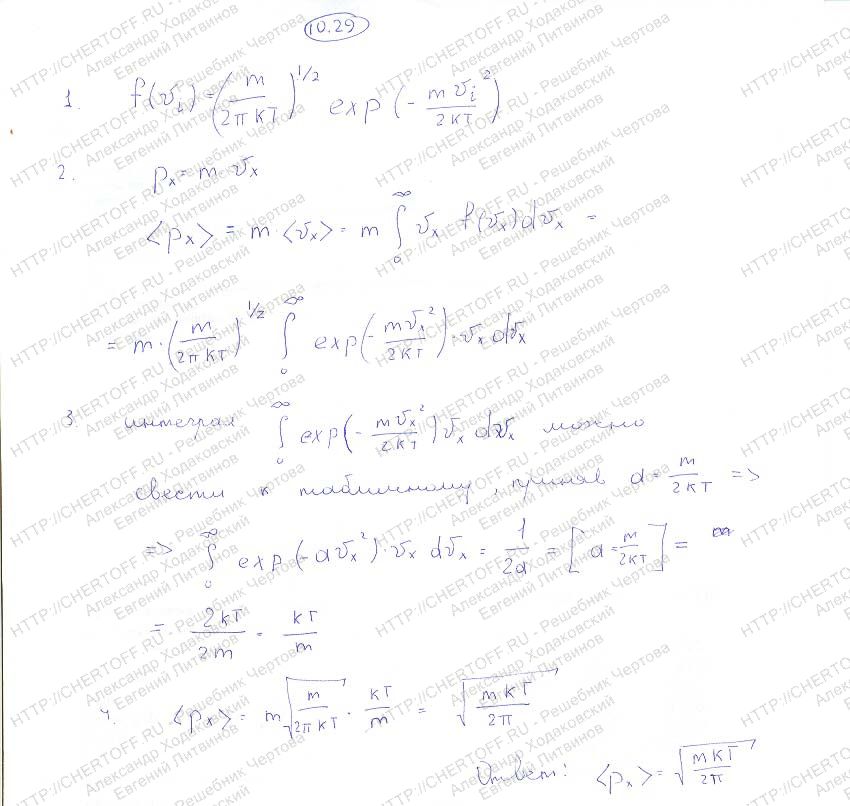


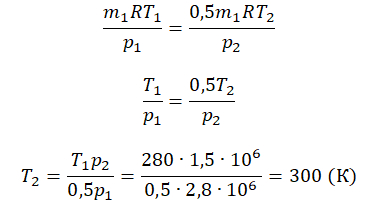
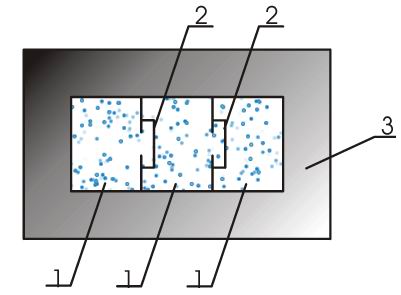



Идеальный газ — это теоретическая модель газа, хорошо описывающая поведение реальных газов при невысоких давлениях и температурах. Для описания его макроскопических параметров температуры, давления и объема используется специальное соотношение, называемое уравнением состояния. Рассмотрим его подробнее. Основное уравнение состояния идеального газа выводится на основе положений молекулярно-кинетической теории.
- Основы физики сжато и понятно. Газовые законы.
- Уравнение состояния идеального газа.
- Идеальным газом называется такой газ , у которого отсутствуют силы взаимного притяжения и отталкивания между молекулами и пренебрегают размерами молекул.
- Для этого нужно использовать равенства. Здесь N — число молекул в сосуде, N А — постоянная Авогадро, m — масса газа в сосуде, M — молярная масса газа.
- Хотя модель идеального газа хорошо описывает поведение реальных газов при низких давлениях и высоких температурах , в других условиях её соответствие с опытом гораздо хуже.
- Они взаимодействуют со стенками сосуда посредствам упругих соударений. Применим неравенства:.



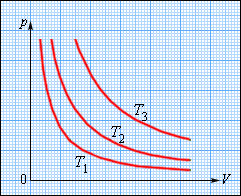
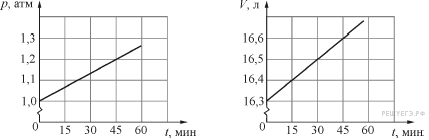
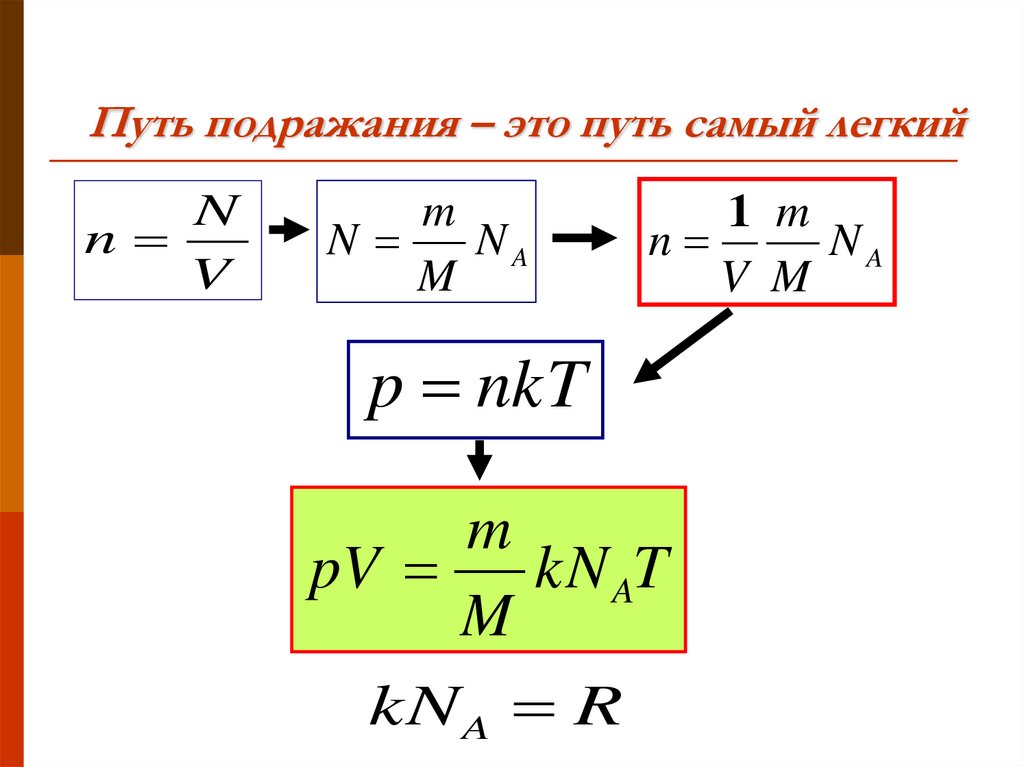


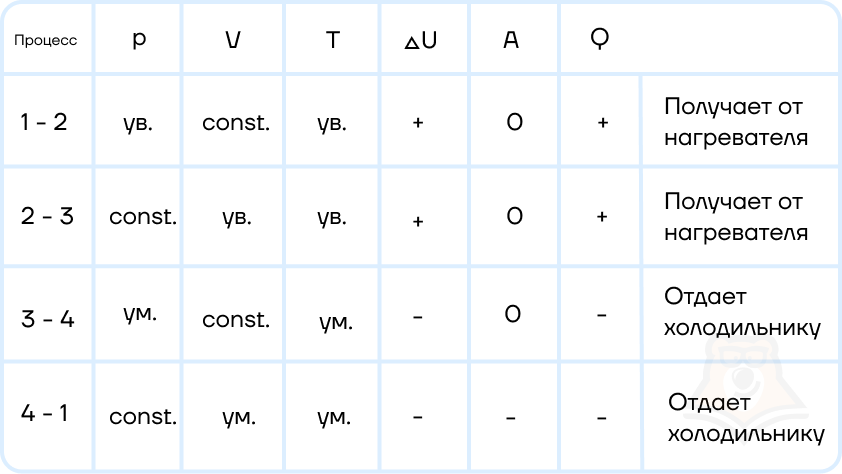
| 189 | Доказательство теоремы. Условия выполнения : выполняется для модели идеального газа, причем масса газа остается неизменной. | |
| 272 | Регистрация Вход. | |
| 137 | Уравнение состояния идеального газа связывает между собой три его макроскопические характеристики — занимаемый газом объём, его давление и температуру. Однако в большинстве случаев пользоваться формулой | |
| 84 | Уравнение состояния идеального газа было открыто экспериментально. | |
| 384 | Учебные материалы по физической химии Реальные газы [предыдущий раздел] [содержание] [следующий раздел] 1. Уравнение Ван-дер-Ваальса Предпринималось много попыток для учета отклонений свойств реальных газов от свойств идеального газа путем введения различных поправок в уравнение состояния идеального газа. | |
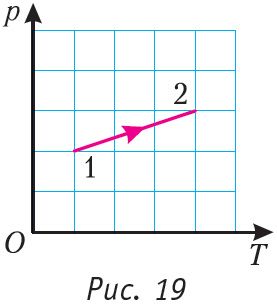
| 486 | Здесь, конечно, речь идёт только о газе, находящемся в состоянии термодинамического равновесия , которое означает, что все макроскопические параметры не изменяются со временем. |
Уравнение имеет вид:. Последнее уравнение называют объединённым газовым законом. С точки зрения химика этот закон может звучать несколько иначе: объёмы вступающих в реакцию газов при одинаковых условиях температуре, давлении относятся друг к другу и к объёмам образующихся газообразных соединений как целые числа. Например, 1 объём водорода соединяется с 1 объёмом хлора , при этом образуются 2 объёма хлороводорода :. В некоторых случаях в газовой динамике уравнение состояния идеального газа удобно записывать в форме.